
微生物+单细胞分选仪 拉曼单细胞分选仪 高通量菌落智能筛选系统 单细胞显微光镊操纵与分选系统 |
拉曼+共聚焦拉曼光谱仪 近红外共聚焦拉曼光谱仪 拉曼单细胞分选仪 |
成像+超快三维荧光成像系统 智能细胞荧光计数仪制药颗粒物检测仪 |
核酸快检便携式核酸恒温扩增分析仪耗材拉曼信号增强芯片 细胞分选芯片 |

微生物+单细胞分选仪 拉曼单细胞分选仪 高通量菌落智能筛选系统 单细胞显微光镊操纵与分选系统 |
拉曼+共聚焦拉曼光谱仪 近红外共聚焦拉曼光谱仪 拉曼单细胞分选仪 |
成像+超快三维荧光成像系统 智能细胞荧光计数仪制药颗粒物检测仪 |
核酸快检便携式核酸恒温扩增分析仪耗材拉曼信号增强芯片 细胞分选芯片 |
使用活细胞成像技术的生物医学研究的爆炸性增长受到一系列事件的推动,包括共焦显微镜仪器的巨大进步、新型超灵敏检测器的引入以及基因编码荧光蛋白性能的持续改进. 在毫秒时间尺度上获取活细胞中局部荧光团的图像,揭示复杂的生物动力学,这带来了许多新的挑战,这些挑战远比传统的问题要复杂得多。为了确保活细胞中荧光蛋白和合成染料的高图像采集速度,具有合理的对比度和最小的光漂白,显微镜必须能够使用具有高量子效率的探测器快速扫描视野并记录数据。激光扫描共聚焦显微镜将单个光束聚焦在样品平面上,以顺序点扫描感兴趣的区域,并通过单个针孔对发射光进行空间过滤。这种方式使图像采集速度受到限制,因为需要极其精确地控制用于光栅扫描样品上的光束的检流计镜,以及样品发射的光子数量有限在像素停留时间。对于一般的成像场景,共聚焦显微镜以每像素 1 ms的速度进行扫描,这意味着每张图像的采集速度在二分之一到两秒之间,具体取决于尺寸。因此,大多数激光扫描共聚焦显微镜不足以捕捉毫秒级的动态事件,而这些事件通常对于解开活细胞中发生的复杂分子过程至关重要。虽然扫描速度的限制可以通过采用共振扫描方案来克服,这种高速采集具有超短的像素停留时间,因此信噪比不足。
与点扫描共聚焦显微镜相关的许多速度限制可以通过使用多个平行操作的激发光束对样品进行成像来克服,即转盘共聚焦显微镜。同时其对光线利用率的提升使得更柔和的LED光源可以替代激光光源,极大降低了观测过程中的光损伤。转盘共聚焦显微镜正在成为活细胞快速空间和时间成像的强大工具。尽管该技术最初是在 40 多年前引入的,但最近在显微镜光学设计和相机技术方面的改进显着扩展了这种方法的多功能性和潜力。
本课题拟开发共聚焦成像清晰度增强算法的主要目的是为了修正共聚焦三维成像存在的模糊与不清楚的问题,并将重要的影像细节呈现,实现生物样品3D结构清晰而准确地成像,观察到活细胞内部的动态变化。
转盘共聚焦显微镜(图1)使用掩膜板限制照明光的范围,同时也阻挡了离焦的光线参与成像,从而大大提高了轴向分辨率(横向分辨率也有一定提升),该种提升使得共聚焦显微镜拥有较窄的轴向响应,对样品进行逐层扫描,在表面的每个点都可以得到图2所示的高斯分布轴向响应曲线,通过高斯拟合寻找最大值可以得到该点的空间高度,进而可以重构样品表面的三维形貌,对其进行表面缺陷检测、粗糙度检测、物理性质分析等。目前市面上的相关仪器横向分辨率可达120-140μm,轴向分辨率1-0.1nm,转盘式扫描方式相比较点扫描方式在少量牺牲的分辨率的情况下极大提升了扫描速度。
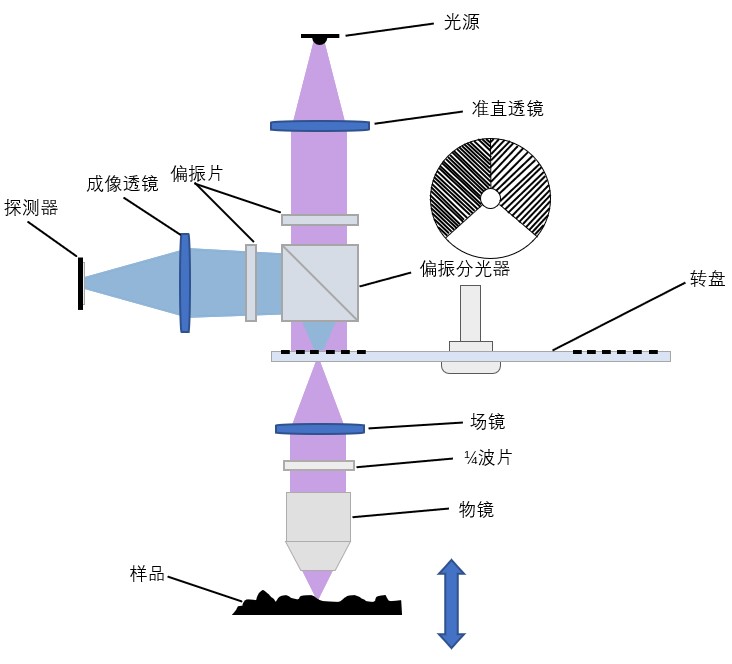
图1 转盘共聚焦原理图

图2 共聚焦轴向响应曲线
在微观图像分析方面,三维成像体系的应用至关重要。由于细胞的形态是肉眼所不能观察的,只能通过显微镜的放大得到序列图像后,然后利用计算机三维重建技术对二维序列图像进行三维重构显示,使细胞结构的三维图像以及不同深度层面的图像得到三维立体的真实形态展现。


 0431-81077008
0431-81077008