《Biomaterials》丨聚合物基因–药物共递送系统抑制病理性视网膜新生血管
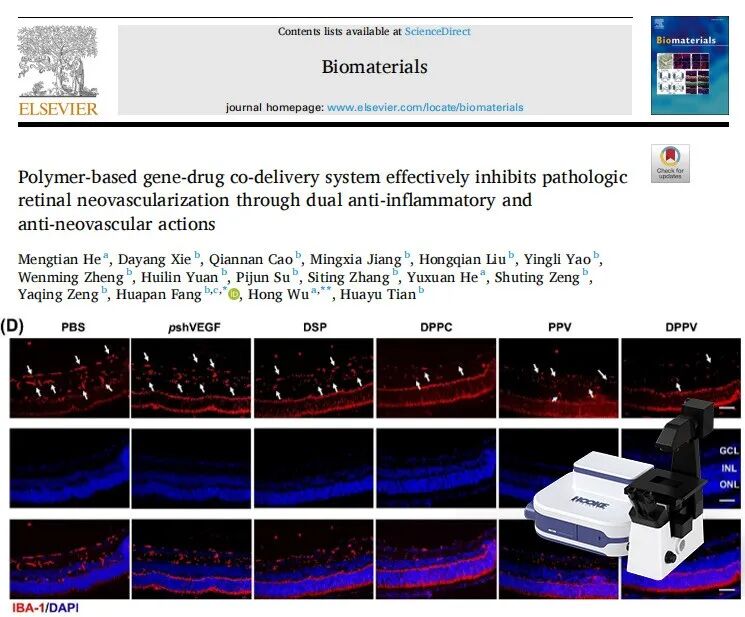
2025 年,吉林大学第二医院吴宏教授团队联合厦门大学研究团队,在《Biomaterials》期刊(影响因子12.9)发表研究论文《Polymer-based gene-drug co-delivery system effectively inhibits pathologic retinal neovascularization through dual anti-inflammatory and anti-neovascular actions》。该研究构建了一种聚合物基因–药物共递送系统,在氧诱导视网膜病变模型中,通过同步抑制血管新生与炎症反应,有效改善病理性视网膜新生血管相关改变。在研究过程中,视网膜整体铺片及切片样本的多标记免疫荧光成像是评估治疗效果与作用机制的重要手段。相关免疫荧光图像由 S3000 超快三维荧光成像系统完成高效采集,为本研究结论提供了关键的高质量成像支持。

病理性视网膜新生血管是多种眼底疾病的重要共同特征,如早产儿视网膜病变、增殖型糖尿病视网膜病变及视网膜静脉阻塞等。异常增生的血管可突破内界膜生长,引发玻璃体出血和牵拉性视网膜脱离,严重威胁视功能。目前临床主要采用抗 VEGF 药物进行玻璃体腔注射治疗,但仍存在需反复给药、部分患者疗效不充分等问题。已有研究表明,视网膜新生血管的发生不仅依赖 VEGF 信号通路,同时伴随显著炎症反应。在缺血或缺氧条件下,促炎因子与 VEGF 协同促进血管内皮细胞增殖与迁移,因此,联合抑制血管生成与炎症反应被认为是提高治疗效果的重要方向。

研究团队设计并构建了一种聚合物基因–药物共递送系统(DPPV)。该体系以苯硼酸修饰的线性聚乙烯亚胺(LPEI-PBA)作为基因载体,负载靶向 VEGF 的 shRNA 质粒(pshVEGF),并协同递送地塞米松磷酸钠(DSP)。研究通过体外实验评估该体系的理化性质、基因转染效率、生物相容性及抗血管生成能力;在体内实验中,构建氧诱导视网膜病变(OIR)小鼠模型,通过单次玻璃体腔注射评估其对病理性视网膜新生血管及炎症反应的抑制效果,并结合组织学与免疫荧光分析进行验证。
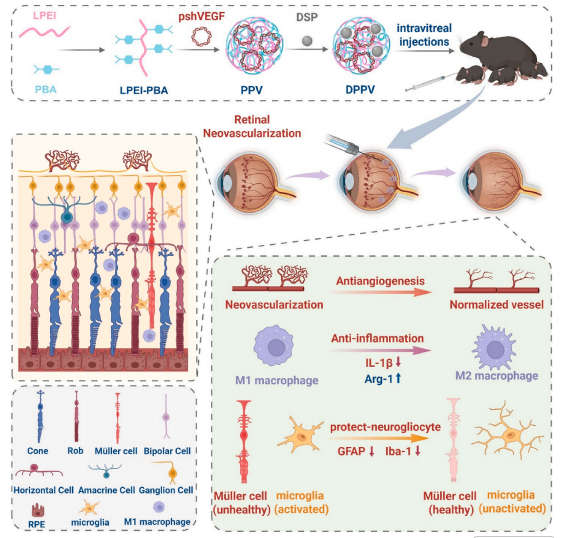
图1. 聚合物基因–药物共递送系统(DPPV)的构建原理及其在氧诱导视网膜新生血管模型中的作用机制示意图
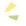

研究首先对共递送体系的构建过程及理化性质进行了表征。结果显示,苯硼酸修饰的线性聚乙烯亚胺可有效负载质粒DNA,并与地塞米松磷酸钠自组装形成稳定的三元复合物。
核磁共振、凝胶阻滞实验及扫描电镜结果表明,该体系具有良好的DNA 负载能力和均一的纳米颗粒形态。粒径与 ζ 电位分析显示,DPPV 颗粒在一定时间范围内保持稳定,为后续实验提供了基础条件。
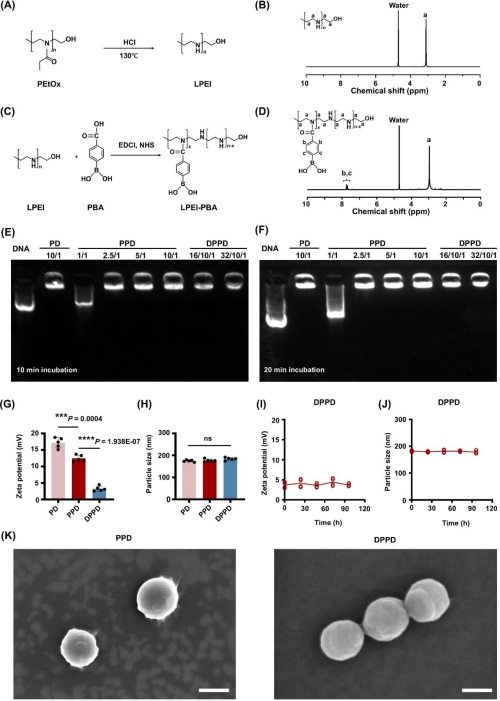
图2. DPPV 共递送体系的合成及理化性质表征
在细胞实验中,研究评估了该体系在视网膜相关细胞中的基因递送能力。结果显示,与未修饰载体相比,LPEI-PBA 可显著提高基因转染效率;在引入地塞米松磷酸钠后,DPPV 的转染效率进一步提升。共聚焦荧光成像与流式细胞术分析表明,DPPV 处理组在 ARPE-19 细胞和 HUVEC 细胞中均表现出更高的细胞摄取效率。同时,在有效剂量范围内,该体系未引起明显细胞毒性,表现出良好的生物相容性。
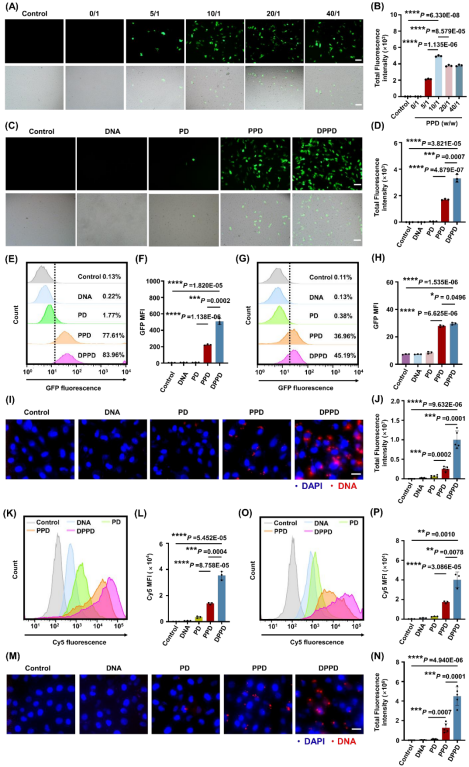
图3. DPPV 体系在视网膜相关细胞中的基因转染效率
与细胞摄取分析
体外功能实验结果显示,DPPV 处理可显著下调内皮细胞中 VEGF 的 mRNA 与蛋白表达水平。在划痕实验、管腔形成实验及脉络膜芽生实验中,DPPV 处理组均表现出显著的血管生成抑制效应,内皮细胞迁移能力及血管网络形成程度明显降低。
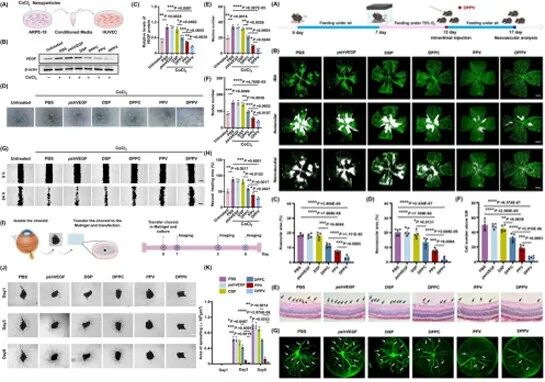
图4. DPPV 处理对体外血管生成相关行为的影响
3.4 DPPV 在 OIR 小鼠模型中抑制病理性视网膜新生血管形成
在OIR 小鼠模型中,单次玻璃体腔注射 DPPV 后,小鼠视网膜病理性新生血管面积显著减少,同时无血管区比例明显降低。视网膜整体铺片及切片分析进一步证实,DPPV 可有效抑制新生血管向玻璃体侧突破内界膜的病理过程,其效果优于单一基因或药物处理组。
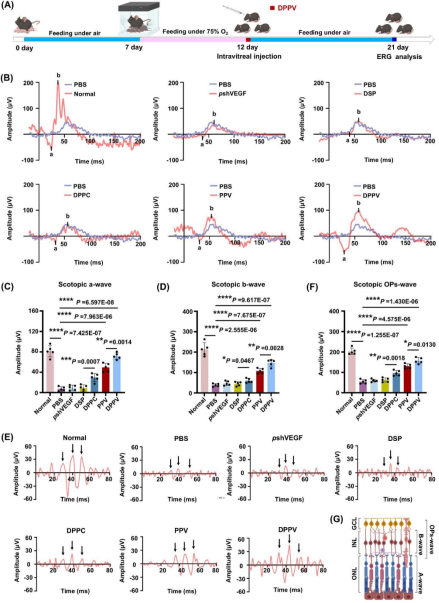
图5. DPPV 在 OIR 小鼠模型中
对病理性视网膜新生血管形成的抑制作用
免疫荧光结果显示,DPPV 处理后,GFAP 与 IBA-1 等胶质细胞激活标志物显著下调,促炎因子 IL-1β 表达降低,而抗炎相关因子 ARG-1 表达上调。同时,视网膜电生理结果提示,DPPV 处理在一定程度上改善了 OIR 小鼠的视功能表现。
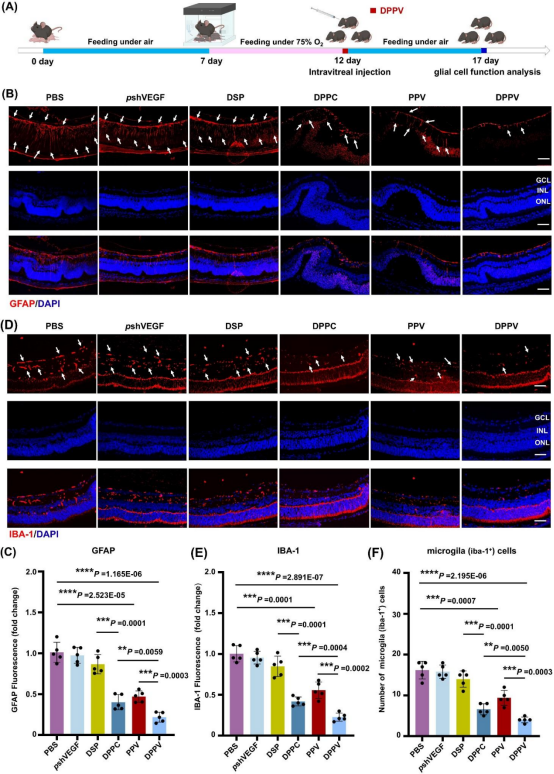
图6. DPPV 处理后视网膜炎症相关标志物
及视觉功能变化

本研究构建并验证了一种聚合物基因–药物共递送系统,可通过抗血管生成与抗炎双重机制,有效抑制病理性视网膜新生血管形成,为相关眼底疾病的治疗提供了一种具有潜力的研究策略。

在本研究中,视网膜整体铺片及切片样本的多标记免疫荧光成像,是评估新生血管形成及炎症反应变化的关键技术环节。研究团队采用S3000 超快三维荧光成像系统 完成相关成像工作。S3000 基于转盘共聚焦成像原理,在保证成像清晰度与信噪比的同时,实现高速、多层面荧光采集,稳定支持视网膜组织中多标志物免疫荧光成像与定量分析,为本研究提供可靠的成像保障。



吴宏
教授,主任医师,医学博士,博士研究生导师,吉林大学第二医院眼科医院副院长,眼底病科主任,长白山特聘领军人才,中国医师协会眼科医师分会眼科药物治疗学组委员,吉林省健康管理学会第一届糖尿病眼病专业委员会副主任委员。《Allergy》中文版编委。曾在新加坡国家眼科中心和新加坡国家科技局工作。在SCI学术期刊上发表了20余篇高质量的SCI文章,主持国家自然科学基金课题和多项省级课题。






