用户文章 | 《Clinical Science》吉林大学第一医院李亚男、张影团队:揭示肺炎克雷伯菌早期感染中外泌体介导的巨噬细胞极化与炎症新机制
近日,吉林大学白求恩第一医院李亚男、张影团队在《Clinical Science》发表研究论文,该研究综合运用单细胞拉曼光谱(Single-cell Raman spectroscopy, SCRS)和外泌体代谢组学技术,深入解析了肺炎克雷伯菌(Klebsiella pneumoniae, K.p.)感染极早期的宿主代谢重编程机制。
长光辰英P300共聚焦拉曼光谱仪通过原位单细胞拉曼成像,在非标记状态下精准捕捉了感染早期宿主细胞的脂质代谢特征变化,为揭示外泌体介导的炎症风暴启动机制提供了关键代谢线索。
研究背景
肺炎克雷伯菌是引起重症肺炎的主要病原体,其临床危害巨大。尽管已有研究关注其致病机制,但关于该菌在感染极早期如何通过改变宿主代谢微环境来诱导剧烈炎症反应的机制尚不明确。现有检测方法难以在单细胞水平原位捕捉宿主细胞的早期代谢改变,限制了对感染启动阶段关键事件的认识。为此,本研究引入单细胞拉曼光谱技术,在无需破坏样本的条件下原位解析感染早期气道上皮细胞的代谢重编程特征,并结合外泌体代谢组学与免疫学分析,系统阐明“病原体-代谢-免疫”轴在肺炎克雷伯菌早期感染中的致病机制。
研究方法
本研究首先利用肺炎克雷伯菌感染气道上皮细胞(BEAS-2B)构建体外感染模型。采用P300共聚焦拉曼光谱仪对感染组织进行原位拉曼成像分析,利用细菌细胞壁肽聚糖的特征峰实现侵入宿主细胞的K.p.免标记空间定位,并通过光谱热图分析感染后不同时间点宿主细胞的代谢特征变化。随后,分离并纯化感染源性外泌体,采用UHPLC-QTOF-MS进行代谢组学分析,鉴定差异代谢物。通过外泌体与巨噬细胞、血管内皮细胞的共培养实验,结合免疫荧光染色、Western blot和qPCR等技术,评估外泌体对巨噬细胞极化和内皮屏障功能的影响。最后,利用体内感染模型验证外泌体介导的炎症损伤效应。
结果
1. 单细胞拉曼光谱原位解析:感染诱导气道上皮“脂质堆积”
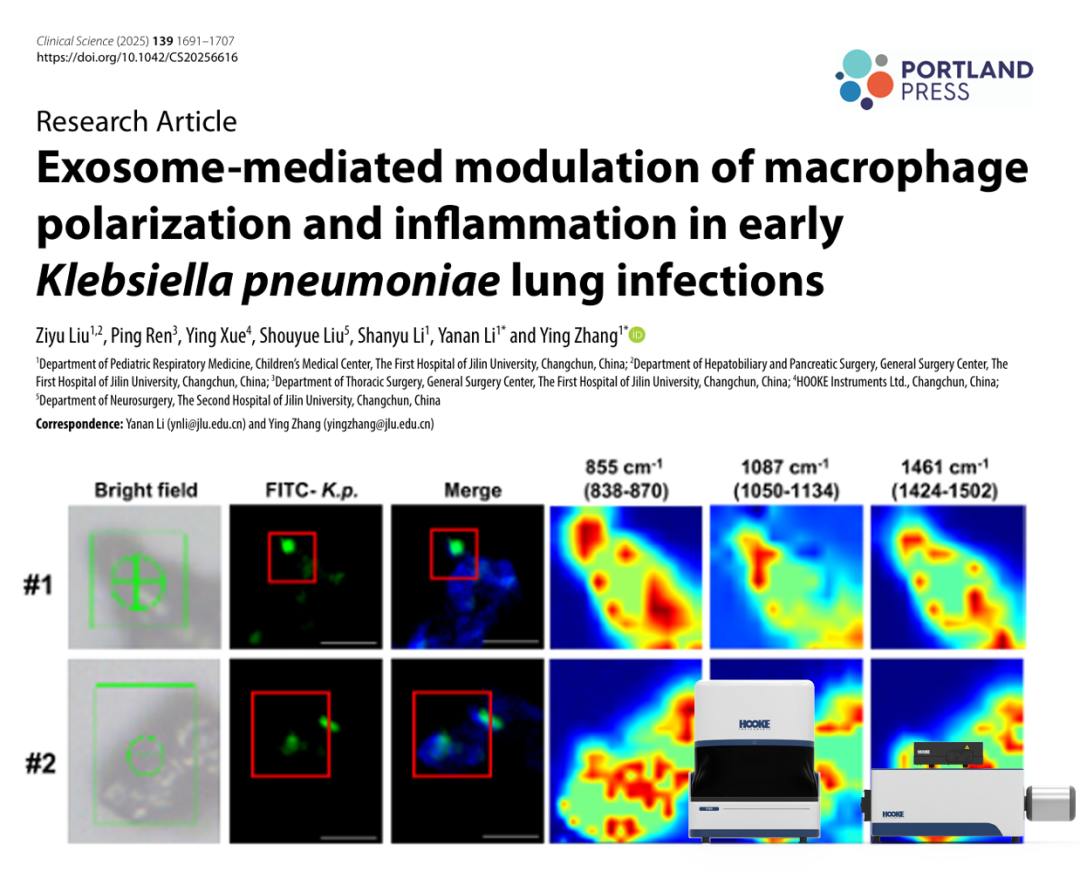
为了在单细胞水平上捕捉K.p.感染引起的早期生化改变,研究团队利用共聚焦拉曼光谱仪对感染组织进行了原位成像分析。 研究利用细菌细胞壁特有的肽聚糖(Peptidoglycan)拉曼特征峰,实现了对侵入宿主细胞内的K.p.进行免标记的空间定位,并与荧光标记结果相互印证。光谱热图显示感染部位在 838–870 cm⁻¹、1050–1134 cm⁻¹ 和 1424–1502 cm⁻¹ 波段的信号显著增强。这些波段对应于脂质(Lipids)中的C-C、CH₂键以及多糖的糖苷键,意味着宿主代谢特征改变。这一结果直观地揭示了K.p.侵染后,气道上皮细胞发生了显著的代谢改变,表现为脂质和多糖成分的异常高表达。这为后续发现“富脂”外泌体的致病机制提供了关键的代谢线索。
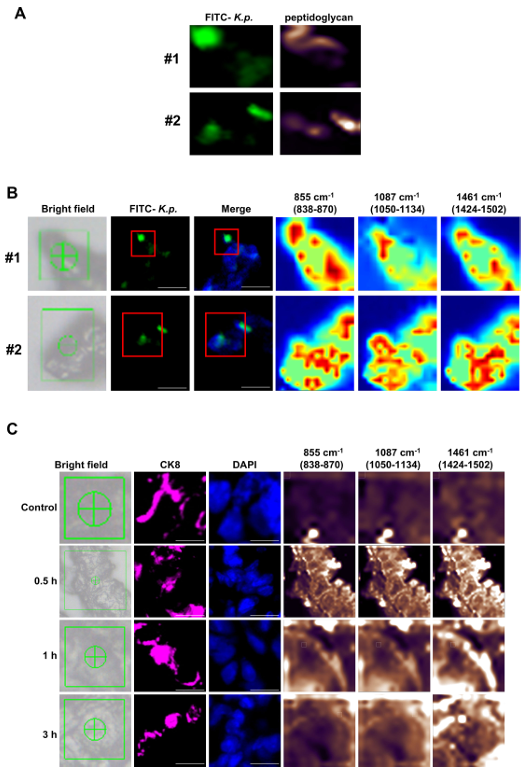
图1.革兰氏阴性杆菌肺炎和肽聚糖的拉曼光谱分析
(A) 拉曼成像显示两个不同样本(#1 和 #2)中的 FITC 标记的肺炎克雷伯菌和肽聚糖。 (B) 两个样本(#1 和 #2)的明场和拉曼光谱图像,显示 FITC-K.p.的分布和相应的拉曼位移。标尺:10 μm。 (C) 感染后不同时间点(对照组、0.5、1、3 小时)肺组织中拉曼光谱变化的时程分析,相应的免疫荧光图像显示 CK8 和 DAPI 染色。标尺:10 μm。
2. “富脂”外泌体:连接上皮感染与血管损伤的信使
基于拉曼光谱发现的脂质代谢异常,团队进一步分离并分析了K.p.感染的BEAS-2B(人支气管上皮细胞)来源的外泌体。 UHPLC-QTOF-MS分析显示,感染源性外泌体中脂质及类脂分子占比高达53.74%。差异代谢物分析进一步锁定磷脂酰胆碱(Phosphatidylcholine)在感染组外泌体中显著富集。这种富含磷脂酰胆碱的外泌体在被血管内皮细胞摄取后,导致紧密连接蛋白 ZO-1 和 Occludin 的表达显著下调,直接破坏了血管内皮屏障的完整性,增加了血管通透性。
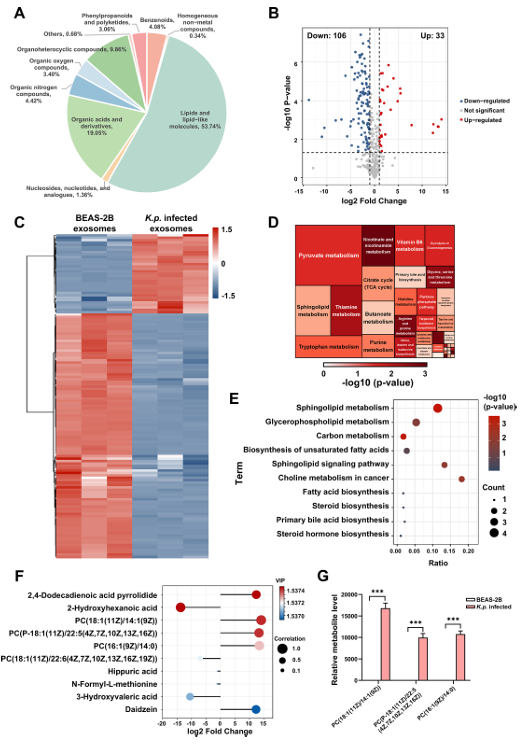
图2.肺炎克雷伯菌感染上皮细胞来源的囊泡代谢组学分析
(A) 外泌体代谢物组成,突出显示脂质和类脂分子是最丰富的类别,其次是有机酸及其衍生物。(B) 火山图显示与对照组相比,肺炎克雷伯菌感染外泌体中代谢物的显著上调和下调。(n=3)。(C) 热图显示 BEAS-2B 外泌体与肺炎克雷伯菌感染细胞外泌体之间代谢物的差异表达。(D) 代谢通路富集分析,在鞘脂和丙酮酸代谢中存在显著结果。(E) 通路分析显示脂质相关代谢通路显著富集,包括鞘脂和甘油磷脂代谢。(F) 前10种差异代谢物的VIP图,突出显示对组间差异有贡献的代谢物。(G) 条形图显示与对照组相比,肺炎克雷伯菌感染外泌体中特定磷脂酰胆碱水平显著增加,表明脂质代谢增强。
3. 免疫调控机制:外泌体驱动巨噬细胞M1极化与炎症风暴
在破坏物理屏障的同时,这些外泌体还充当了免疫系统的“促炎剂”。共培养实验证实,感染源性外泌体能够被巨噬细胞摄取,诱导其显著上调iNOS 和 CD86 等M1型标志物,促进巨噬细胞向促炎表型分化。机制研究表明,外泌体进入巨噬细胞后,诱导了 NF-κB p65 的磷酸化及核转位。NF-κB通路的激活进一步促进了促炎细胞因子(TNF-α, IL-6)和趋化因子(CXCL1, CXCL2)的释放。这些趋化因子随后在体内实验中被证实能大量招募中性粒细胞浸润肺部,导致严重的组织损伤。
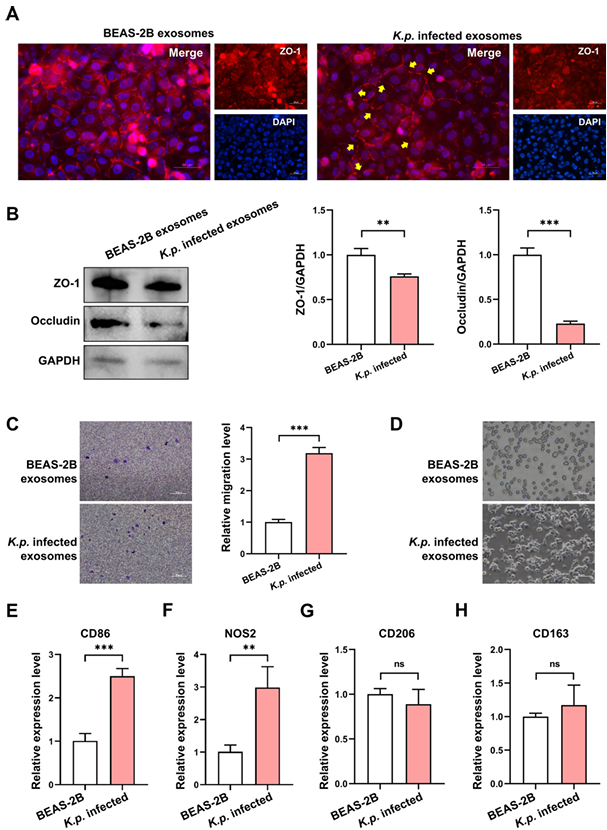
图3.克雷伯氏肺炎菌感染外泌体对内皮屏障和巨噬细胞极化的影响
(A) 免疫荧光图像显示HUVEC细胞在经肺炎克雷伯菌感染外泌体处理后 ZO-1 表达减少,表明紧密连接被破坏。标尺:50 μm。(B) Western blot 分析比较对照组,量化 HUVEC 细胞与肺炎克雷伯菌感染外泌体共孵育后ZO-1和occludin表达的降低。**P<0.01, ***P<0.001(n = 3)。(C) Transwell 实验显示与肺炎克雷伯菌感染外泌体共培养时巨噬细胞浸润增强。标尺:50 μm。(D) 与对照组相比,经肺炎克雷伯菌感染外泌体处理的巨噬细胞形态变化,显示更明显的拉长。标尺:50 μm。(E-H) 巨噬细胞极化标志物的 qPCR 分析。CD86 和 NOS2 表达的增加表明极化向 M1 巨噬细胞发展,而 CD206 和 CD163 水平保持不变。**P<0.01, ****P<0.0001, ns:无显著差异(n = 3)。
结论
本研究描绘了K.p.早期肺部感染的一条完整的“病原体-代谢-免疫”轴:
1.早期侵袭与代谢改变:K.p. 侵入气道上皮细胞,拉曼光谱原位检测证实细胞内出现脂质和多糖的异常积聚;
2.外泌体释放:受感染的上皮细胞释放富含磷脂酰胆碱的外泌体;
3.双重致病效应:对内皮细胞, 破坏ZO-1/Occludin,瓦解血管内皮屏障;对巨噬细胞,被吞噬后激活NF-κB信号通路,驱动M1极化;
4.炎症爆发:释放趋化因子,招募中性粒细胞,导致急性肺炎症。
研究揭示了外泌体介导的磷脂酰胆碱传递是K.p.感染诱导炎症风暴的关键环节,阻断这一外泌体通讯或干预脂质代谢可能为治疗重症肺炎提供新的策略。
辰英价值
在本研究中,长光辰英P300共聚焦拉曼光谱仪凭借其高分辨率拉曼成像与高灵敏度光谱检测能力,成功实现了肺炎克雷伯菌早期感染中宿主细胞代谢特征的原位解析。该仪器的非标记、无损检测特性使得样本结构得以完整保留,避免了传统标记方法的干扰。P300能够在单细胞水平精准识别脂质与多糖的特征拉曼峰,并通过光谱热图直观展示感染后宿主细胞的“脂质堆积”现象。这一发现为后续揭示“富脂”外泌体的致病机制提供了关键的代谢线索,充分体现了P300作为“代谢显微镜”在感染病理学研究中的重要应用价值。其内置的智能分析软件支持深度数据挖掘,为解析病原体-宿主互作的早期代谢事件提供了强有力的工具支撑。

团队介绍

李亚男
吉林大学第一医院小儿呼吸科教授、博士生导师,科室副主任。主持多项国家自然科学基金项目及省部级科研项目;以第一完成人获吉林省自然科学二等奖。近年来以第一作者或通讯作者发表SCI论文20余篇,研究方向聚焦儿童呼吸系统感染性疾病。兼任中华医学会儿科感染学组委员等多个学术职务。临床思维灵活,擅长疾病分析与诊断,新冠疫情期间组建吉林省首个儿童新冠病毒感染治疗专区,获央视新闻报道。
张影
吉林大学第一医院副主任医师。长期从事感染性疾病的基础与转化研究,聚焦于病原体与宿主互作机制、感染微环境代谢重编程及新型抗感染策略开发。近年来,综合运用单细胞拉曼光谱、代谢组学与免疫学等多学科技术,系统解析了多种病原菌早期感染的分子机制。相关研究成果发表于Clinical Science、Emerging Microbes & Infections 等国际期刊。主持多项国家级及省部级科研项目。







